Un fragmento de petavóxel de la corteza cerebral humana reconstruido a resolución nanométrica.
- Consejo Mexicano Neurociencias

- 17 mar
- 32 Min. de lectura
ALEXANDER SHAPSON-COE. MICHAt JANUSZEWSKI, DANIEL R. BERGER, ART POPE, YUELONG WU, IIM BLAKELY, RICHARD L. SCHALEK, PETER H. LI, SHUOHONG WANG [...], AND JEFF W. LICHTMAN
SCIENCE • 10 May 2024 • Vol 384, Issue 6696 • DOI: 10.1126/science.adk4858
INTRODUCCIÓN
Si bien las funciones de la mayoría de los órganos vitales humanos no difieren mucho de las de otros animales, las del cerebro humano nos distinguen claramente del resto de la vida en el planeta. Sin embargo, se carece de un conocimiento detallado sobre los circuitos sinápticos que subyacen a la función cerebral humana. Actualmente, existen técnicas de imagen conectómica que permiten visualizar circuitos neuronales con un volumen suficientemente grande y una resolución lo suficientemente alta como para estudiar la conectividad a nivel de neuronas individuales y sus conexiones sinápticas, pero a una escala que abarca miles de neuronas. Generar un conjunto de datos de este tipo fue el objetivo de este proyecto.
FUNDAMENTO
Una barrera crucial para obtener circuitos neuronales humanos ha sido el acceso a tejido cerebral humano de alta calidad. Las biopsias de órganos proporcionan información valiosa sobre muchos sistemas orgánicos humanos, pero rara vez se realizan en el cerebro, salvo para examinar o extirpar masas neoplásicas, por lo que la mayoría resultan problemáticas para la investigación de la estructura cerebral humana normal. Un intento ha consistido en utilizar organoides cerebrales creados a partir de células humanas, pero actualmente no reproducen la arquitectura del tejido cerebral (por ejemplo, carecen de capas corticales). Un enfoque directo sería mapear las células y los circuitos a partir de muestras humanas obtenidas de intervenciones neuroquirúrgicas para afecciones neurológicas, en las que se desechan fragmentos de la corteza porque obstruyen el acceso a la zona patológica. Planteamos la hipótesis de que el tejido cerebral humano, subproducto de los procedimientos neuroquirúrgicos, podría utilizarse para estudiar los circuitos neuronales humanos normales y, en última instancia, los patológicos.
RESULTADOS
Aquí describimos una muestra de corteza temporal humana, de 1 mm³ de volumen, que abarca todas las capas corticales. La muestra se obtuvo durante una cirugía para acceder a una lesión hipocampal subyacente en un paciente con epilepsia.
Obtuvimos imágenes de esta muestra mediante microscopía electrónica de secciones seriadas de alto rendimiento, generando un conjunto de datos a escala petaflop que se analizó con nuevas herramientas y métodos computacionalmente intensivos. Reconstruimos miles de neuronas, más de cien millones de conexiones sinápticas y todos los demás elementos tisulares que componen la materia cerebral humana, incluyendo células gliales, vasos sanguíneos y mielina.
Debido a que el conjunto de datos es extenso y aún no se ha analizado en profundidad, compartimos todos los datos en un recurso en línea (https://h01-release.storage.googleapis.com/land-ing.html) y también proporcionamos herramientas para su análisis y revisión. Encontramos una clase de neuronas con orientación direccional previamente desconocida en capas profundas (véase la figura, panel J) y conexiones multisinápticas muy potentes y poco frecuentes entre neuronas en toda la muestra (véase la figura, panel K).
CONCLUSIÓN
Este trabajo demuestra la viabilidad de los enfoques conectómicos humanos para visualizar y, en última instancia, comprender las bases físicas del funcionamiento cerebral humano, tanto normal como patológico. Se espera que este esfuerzo se vea facilitado por el acceso gratuito a todos los datos y herramientas relevantes.


Conjunto de datos compartido H01. Se representaron diversas características histológicas en 1 mm² de cerebro humano, incluyendo el neuropilo (A) y su segmentación (B) con resolución nanométrica, sinapsis anotadas (C), neuronas excitadoras (D), neuronas inhibidoras (E), astrocitos (F), oligodendrocitos (G), mielina (H) y vasos sanguíneos (I). También se identificó una clase neuronal previamente no reconocida (J) y conexiones multisinápticas (K).
Resumen
Para comprender plenamente el funcionamiento del cerebro humano, es necesario conocer su estructura con alta resolución. Aquí se presenta una reconstrucción computacionalmente intensiva de la ultraestructura de un milímetro cúbico de corteza temporal humana, extirpado quirúrgicamente para acceder a un foco epiléptico subyacente. Contiene aproximadamente 57 000 células, unos 230 milímetros de vasos sanguíneos y unos 150 millones de sinapsis, con un tamaño de 1,4 petabytes. Nuestro análisis mostró que la glía supera en número a las neuronas en una proporción de 2:1, los oligodendrocitos son las células más comunes, las neuronas excitadoras de las capas profundas se pueden clasificar según la orientación dendrítica y, entre miles de conexiones débiles a cada neurona, existen raras y potentes entradas axónicas de hasta 50 sinapsis. Futuros estudios que utilicen este recurso podrían aportar información valiosa sobre los misterios del cerebro humano.
Se dispone de muestras de tejido cerebral humano de alta calidad procedentes de intervenciones neuroquirúrgicas en personas vivas a las que se les extirpó parte de la corteza cerebral debido a que obstruía el acceso a una región patológica. Aquí describimos una de estas muestras: una lámina de corteza cerebral humana de 170 µm de espesor, conservada rápidamente (véase la sección de materiales y métodos), procedente de la parte anterior de la circunvolución temporal media de una mujer de 45 años. La muestra tiene un volumen total de poco más de 1 mm³ y se extrajo para acceder a un foco epiléptico en el hipocampo subyacente. Una advertencia importante relacionada con las muestras quirúrgicas humanas es que provienen de personas con patologías del sistema nervioso, como epilepsia, tumores o enfermedades neurodegenerativas. En este caso, no podemos descartar la posibilidad de que la epilepsia a largo plazo, o su tratamiento farmacológico, haya tenido efectos sutiles en la estructura a escala nanométrica de la muestra. Sin embargo, al menos según el examen neuropatológico basado en microscopía óptica, la muestra se consideró normal, careciendo, por ejemplo, de la banda de neuronas agregadas que se observa en la parte externa de la capa 2 cuando la esclerosis del hipocampo asociada con la epilepsia se extiende al lóbulo temporal adyacente (26).
Buscamos reconstruir una muestra humana que abarcara las seis capas de la corteza, con un espesor aproximado de 3 mm desde la capa 1 hasta la sustancia blanca. Las limitaciones de rendimiento de la microscopía electrónica de secciones seriadas restringieron el espesor total de la muestra reconstruida. Sin embargo, dado que la muestra está orientada perpendicularmente a la piamadre y sigue la dirección de ramificación de los axones y dendritas principales de las neuronas piramidales, muchos de estos pudieron ser rastreados a través de las capas corticales. La adquisición, alineación computacional, segmentación tridimensional (3D) automatizada y anotación sináptica automatizada de tejido cerebral humano digital a esta gran escala y con alta resolución no solo permite el acceso a circuitos neuronales que comprenden miles de neuronas y millones de sinapsis, sino que también proporciona una visión clara de todos los demás elementos tisulares que componen la materia cerebral humana, incluidas las células gliales y la vasculatura sanguínea, y de las relaciones entre los diversos tipos de células. De este modo, una amplia gama de preguntas relacionadas con la biología del cerebro humano pueden ser analizadas a partir de una sola muestra, a la que hemos denominado H01. Para facilitar su análisis, compartimos todos los datos de H01 y las herramientas utilizadas para analizarlos en un recurso en línea: https://h01-elease.storage.googleapis.com/landing.html.
Muestra cerebral reconstruida La muestra que analizamos proviene del giro temporal medio anterior izquierdo, resecado para acceder a un foco epiléptico subyacente. Se sometió a fijación rápida, se tiñó con metales pesados (27) y se incluyó en resina. Posteriormente, se obtuvieron 5019 secciones con un grosor medio de 33,9 nm, que se colocaron en cinta adhesiva (28), lo que dio como resultado un grosor total de 170 µm (véase la sección de materiales y métodos). Cada sección se visualizó mediante microscopía electrónica de barrido multihaz con una resolución de 4 × 4 nm (Fig. 1A y tabla S1) y se alineó (Fig. 1B), lo que generó un conjunto de datos de aproximadamente 1,4 petabytes y 1,05 mm³ de volumen tras corregir la compresión tisular inducida por el seccionamiento (véase la sección de materiales y métodos).

Fig. 1. Conjunto de datos H01, adquisición de imágenes y alineación.
(A) Una muestra fresca de corteza cerebral humana obtenida mediante cirugía se conservó rápidamente, se tiñó, se incluyó en resina, se seccionó a ~33 nm, se recogió en cinta adhesiva y se analizó mediante el método ATUM-MSEM (microscopía electrónica de barrido multihaz). El microscopio electrónico Zeiss mSEM utiliza 61 haces que capturan imágenes de un área hexagonal de ~10 000 µm² simultáneamente, lo que permite analizar grandes áreas rápidamente. Para cada sección, todas las teselas resultantes se unieron (izquierda); esta sección tiene un área de ~4,5 mm² y se analizó con píxeles de 4 × 4 nm². La imagen de la sinapsis se muestra a la derecha. Dada la necesidad de cierta superposición entre las teselas unidas, esta única sección requirió la recopilación de más de 300 gigabytes de datos. (B) Alineación a escala fina con flujo óptico. Izquierda: una sección transversal x-y del subvolumen inicial con alineación aproximada muestra deriva y fluctuación. Centro: dos secciones XY adyacentes, z (verde) y z-1, se superponen para ilustrar su desalineación. La correlación cruzada basada en parches de imagen calcula un campo de flujo x-y entre ellas. Las intensidades roja y azul, que indican los componentes de flujo horizontal y vertical respectivos, se utilizaron para deformar una de las secciones, mejorando su alineación (superposición de relajación y deformación). Derecha: vista x-z del mismo subvolumen con realineación de flujo aplicada.
Generamos una reconstrucción 3D de casi todas las células y procesos en el volumen alineado mediante una red de relleno por inundación (FFN) multirresolución (29). Esto produjo fragmentos de objetos completos (segmentos base), que luego se aglomeraron para producir objetos más grandes, incluyendo cuerpos celulares con axones y dendritas (Fig. 2, A y B; véase la sección de materiales y métodos). Sin embargo, este proceso de aglomeración generó errores de fusión entre objetos cercanos, como un axón y una dendrita que se superponían, los cuales, en muchos casos, pudieron corregirse mediante la clasificación automática de los objetos (Fig. 2C; véase la sección de materiales y métodos). Debido a la disyuntiva entre eliminar errores de división y añadir errores de fusión, generamos dos agrupaciones diferentes en la plataforma en línea Neuroglancer (https://h01-dot-neuroglancer-demo.appspot.com/#!gs://h01-release/asets/neuroglancer_states/20230907/c2_vs_c3.json). La agrupación c2 favoreció menos errores de división (y, por lo tanto, procesos más largos) pero con un mayor número de errores de fusión. Por el contrario, la agrupación c3 tuvo más errores de división pero menos errores de fusión. Al revisar las neuronas en Neuroglancer (https://h01-dot-neuroglancer-demo.appspot.-com/#!gs://h01-release/assets/neuroglancer_states/20230907/proofread_cells.json; véase la tabla S2 y los materiales y métodos), observamos que la aglomeración c3 requería 1,6 veces menos corrección de errores de fusión (257 frente a 400 operaciones de corrección de fusión por célula, P < 10⁻⁷, n = 10⁴, prueba t de Student para muestras pareadas), pero 2,1 veces más corrección de errores de división (504 frente a 238 operaciones de corrección de división por célula, P < 10⁻¹⁰, n = 10⁴, prueba t de Student para muestras pareadas) en comparación con la aglomeración c2 (excluyendo las espinas dendríticas). Los errores de división no se distribuyeron uniformemente en el volumen H01 (fig. S1; véase la sección de materiales y métodos), como se muestra al mapear la tendencia (azul: alta, rojo: baja) de los segmentos en la aglomeración c3 a atravesar capas z consecutivas en Neuroglancer. Los errores de fusión en la segmentación de la base en sí fueron raros, observándose solo en 13 de 365.404 segmentos de base que comprenden las neuronas de corrección (0,0036%). Todos los análisis posteriores en el presente estudio se basaron en el c3.

Centro: los campos de visión alrededor de un subconjunto de nodos del esqueleto se introducen en un modelo de clasificación de subcompartimentos. Los nodos rojos muestran una dendrita predicha; Los nodos azules muestran un axón predicho. Se detecta la inconsistencia en las predicciones de subcompartimentos y el gráfico de aglomeración se corta en la ubicación que mejora al máximo la consistencia de los subcompartimentos. Derecha: el axón y la dendrita separados después de aplicar el corte sugerido; se puede ver una representación 3D de los fragmentos separados con predicciones de subcompartimentos en Neuroglancer (https://h01-dot-neuroglancer-demo.appspot.com/#!gs://h01-release/assets/neuroglancer_states/20240424/fig2c.json). (D) Detección y clasificación de sinapsis. Arriba: sección transversal X-Y de la entrada de la imagen EM al modelo de detección de sinapsis (izquierda) y las máscaras de predicción presinápticas (magenta) y postsinápticas (verde) resultantes (derecha). Abajo: sección transversal de la imagen de EM y entradas de segmentación de objetos presinápticos (izquierdo rojo, derecho azul) y postsinápticos (verde) al modelo de clasificación excitatorio versus inhibitorio. Derecha: representación 3D de una dendrita con sitios sinápticos excitatorios (amarillo) e inhibitorios (azul) predichos; una representación 3D de todas las entradas a esta neurona se puede ver en Neuroglancer (https://h01-dot-neuroglancer-demo.appspot.com/#!gs://h01-release/assets/neuroglancer_states/20210601/figs/fig2d.json).
Predicción de sinapsis
La identificación de sinapsis fue necesaria para analizar la conectividad entre neuronas en este conjunto de datos. Como se muestra en la Figura 2D, utilizamos herramientas de aprendizaje automático para entrenar clasificadores automáticos de sinapsis que identificaran el componente pre y postsináptico de cada sinapsis y determinaran si el terminal presináptico era excitatorio o inhibitorio (véase la sección de materiales y métodos). La revisión manual de una selección de axones que abarcan todas las capas corticales mostró que el número de sinapsis no detectadas (falsos negativos) para sinapsis excitatorias e inhibitorias fue del 11 % y del 35 %, respectivamente. La tasa de falsos positivos para sinapsis excitatorias e inhibitorias fue del 3,2 % y del 2,7 %, respectivamente (Tabla S3). En total, se detectaron automáticamente 149.871.669 sinapsis en el volumen. Un total de
111.272.315 sinapsis se clasificaron como excitatorias y 38.599.354 como inhibitorias. Según la revisión, las sinapsis excitatorias e inhibitorias se clasificaron correctamente el 86,89 % y el 84,98 % de las veces, respectivamente. Ajustando las tasas medidas de falsos descubrimientos, falsos negativos y errores de clasificación excitatoria o inhibitoria, estimamos que el volumen H01 contiene un total de 102,5 millones (67,1 %) de sinapsis excitatorias y 50,3 millones (32,9 %) de sinapsis inhibitorias. Analizando el componente postsináptico de 133.704.881 de las sinapsis identificadas automáticamente (véase la sección de materiales y métodos), encontramos, como era de esperar, un alto porcentaje de estas sinapsis ubicadas en las dendritas (99,4 %), con muchas menos inervando los segmentos iniciales del axón (AIS, 0,197 %) o los somas (0,394 %).
Herramientas para la reconstrucción celular y la exploración de circuitos
Si bien algunos análisis de los datos no se verán afectados por los errores de aglomeración, división y fusión descritos anteriormente, otros análisis, en particular los que se realizan a nivel de circuitos neuronales, requieren la corrección de estos errores mediante la revisión. Debido a la gran cantidad de estructuras neuronales, resulta inviable que un solo laboratorio revise manualmente todo el conjunto de datos. Para facilitar los estudios científicos que requieren la corrección de errores de aglomeración mediante la revisión, ofrecemos una plataforma colaborativa de revisión en línea para H01 (https://h01-release.storage.googleapis.com/proofread-ing.html), basada en la infraestructura CAVE (Connectome Annotation and Versioning Engine) (30). Esta herramienta web está integrada con el visor Neuroglancer. Los revisores pueden actualizar interactivamente la segmentación corrigiendo los errores de fusión y división. Todos los revisores tienen acceso a la segmentación más actualizada en todo momento para evitar ediciones redundantes por parte de varios miembros de la comunidad. Seleccionamos la aglomeración c3 como punto de partida para el proceso de revisión colaborativa.
Cualquier persona puede solicitar ser revisor, y los revisores pueden descargar los datos relacionados con las células que han revisado para análisis posteriores, como se muestra en los tutoriales en línea (https://github.com/VCG/cave-scripts). La versión más reciente del volumen revisado siempre está disponible para su consulta en Neuroglancer (https://ngl.brain-wire.org/#!gs://h01-release/assets/neuroglancer_states/cave/demo.json) para cualquier investigador interesado, sin necesidad de solicitar ser revisor.
VAST (Volume Annotation and Segmentation Tool) (31) es una herramienta de software libre y versátil (https://lichtman.rc.fas.harvard.edu/vast/) que permite visualizar, segmentar y anotar grandes conjuntos de datos de vóxeles. A diferencia del sistema CAVE descrito anteriormente, que se centra principalmente en la corrección de errores de división y fusión de la segmentación aglomerada, VAST permite generar nuevas segmentaciones de referencia de objetos de interés (p. ej., vasculatura u orgánulos) mediante la pintura manual de vóxeles y crear esqueletos binarios anotados para análisis cuantitativos (p. ej., mediciones de volumen o longitud). VAST también permite aglomerar localmente segmentos c2 o c3. Para que los datos de imagen H01 estén disponibles en VAST, ampliamos el programa para que lea los datos directamente desde el almacenamiento en línea compatible con Neuroglancer. Los resultados de VAST se pueden exportar en varios formatos para su análisis y visualización. VAST también incluye una interfaz de programación de aplicaciones (API) que permite la automatización mediante scripts con Matlab. VAST se utilizó para obtener varios resultados en este estudio, incluido el etiquetado y la clasificación manual de todos los cuerpos celulares que se describen a continuación.
Para el análisis, se encuentran disponibles varias bases de datos en el recurso en línea HO1 (https://h01-release.storage.googleapis.com/data.html) que permiten realizar consultas específicas sobre los datos celulares y sinápticos. Sin embargo, estas no están integradas con la plataforma Neuroglancer y no admiten consultas más complejas a nivel de red neuronal. Para solucionar esto, desarrollamos un programa independiente, CREST (Connectome Reconstruction and Exploration Simple Tool). CREST se puede utilizar para identificar y explorar las conexiones de las células en función de varias de sus características, incluyendo el número de entradas o salidas sinápticas de una determinada intensidad (véase la descripción de conexiones sinápticas fuertes más adelante). CREST también se puede utilizar para explorar y graficar cadenas de neuronas conectadas sinápticamente, determinando cómo la influencia postsináptica de una neurona diverge a través de múltiples generaciones de neuronas posteriores y cómo convergen las influencias presinápticas de múltiples generaciones de neuronas anteriores. Cabe destacar que las rutas identificadas de esta manera requieren verificación manual debido a la presencia de errores de fusión de aglomeraciones y, en menor medida, falsos positivos de sinapsis. Las rutas verificadas de interés pueden guardarse localmente, junto con la vista esquemática de la ruta, para su posterior revisión con la herramienta CREST. Finalmente, CREST también incluye una herramienta de corrección que permite revisar las células y guardar localmente cada versión de una célula. Las instrucciones detalladas para el usuario y el programa CREST están disponibles en la página principal de CREST (https://github.com/ashapsoncoe/CREST).
Organización celular y sináptica
El volumen segmentado completo (Fig. 3), incluidas las anotaciones sinápticas y de subcompartimentos, está disponible para su exploración en la plataforma Neuroglancer. Un vídeo demostrativo sobre cómo explorar las distintas superposiciones de datos, modificar su apariencia y navegar por el conjunto de datos H01 está disponible en línea.

Figura 3. Volumen H01 segmentado.
Izquierda: Vista oblicua del conjunto de datos H01 tras todos los pasos de segmentación automática, recortado al volumen completo y estirado para compensar la compresión de la sección debida al seccionamiento ultrafino. La autosegmentación C3 se muestra superpuesta en colores aleatorios. Derecha: Recorte del conjunto de datos en la ubicación del rectángulo rojo que muestra una sección transversal de la pila de imágenes alineadas. Las líneas rosas indican el punto de unión de las dos series de seccionamiento (fase 1 y fase 2).
El recurso H01 se divide en numerosas subcategorías. Basándonos en clasificaciones de nodos del esqueleto y anotaciones manuales, y excluyendo espacios extracelulares, vainas de axones mielinizados y artefactos tisulares (véase la sección de materiales y métodos), el neuropilo, en términos de volumen, se compone de axones amielínicos (~40,2 %), dendritas (~25,8 %), prolongaciones gliales (~15,5 %), somas (~9,4 %), axones mielinizados sin sus vainas (~7,5 %), vasos sanguíneos colapsados (~1,5 %), AIS (~0,07 %) y cilios (~0,03 %) (véase también la tabla S4 para el desglose por capa cortical). Además de estas categorías bien conocidas, encontramos varios objetos corticales no identificados que representaban un volumen muy reducido (fig. S2).
Analizamos todas las células con núcleo en la muestra (fig. 4), identificándolas y cuantificándolas manualmente (tablas S5 y S6). Se observaron 49 080 neuronas y células gliales (Fig. 4A) y 8100 células relacionadas con vasos sanguíneos (57 180 células en total; Fig. 4B). Las células gliales superaban en número a las neuronas en una proporción de 2:1 (32 315 frente a 16 087). De las neuronas, el 65,5 % eran espinosas (10 531, de las cuales 8803 tenían forma piramidal), el 29,1 % no eran espinosas ni piramidales y, por lo tanto, se clasificaron como interneuronas (4688), y el 5,4 % (868) no encajaban fácilmente en esta categorización binaria, principalmente porque sus somas no se encontraban completamente dentro del volumen. También se observaron algunas neuronas inusuales difíciles de clasificar; en la figura S3 se muestran ejemplos de esta última categoría. En general, la densidad de neuronas fue de aproximadamente 16 000/mm², aproximadamente un tercio menor que la estimada previamente mediante microscopía óptica de la corteza temporal humana (33) y casi 10 veces menor que la densidad de la corteza de asociación del ratón (34-36).

Figura 4. Distribución de células, vasos sanguíneos y mielina en la muestra.
Las líneas blancas indican los límites de las capas según la agrupación celular. (A) Los 49 080 cuerpos celulares de neuronas y células gliales de la muestra, coloreados según el volumen del soma. (B) Vasos sanguíneos y núcleos de las 8136 células asociadas; se pueden visualizar representaciones 3D de todos los vasos sanguíneos en Neuroglancer (https://h01-dot-neuroglancer-demo.appspo
t.com/#!gs://h01-release/assets/neuroglancer_states/20240424/fig4b.json). El recuadro muestra una vista ampliada de la ubicación de cada tipo celular. (C) Neuronas espinosas (n = 10 531; presuntamente excitadoras), coloreadas según el volumen del soma. (D) Interneuronas (n = 4688; pocas espinas, presuntamente inhibidoras), coloreadas según el volumen del soma. (E) Astrocitos (n = 5474). (F) La mayoría de los oligodendrocitos (n = 20 139) en el volumen. (G) Cuerpos celulares (n = 6702) de microglía y OPC. (H) Axones mielinizados en el volumen, codificados por color según su orientación topológica. La mayoría de los axones en la sustancia blanca discurren perpendicularmente. Las imágenes y la barra de escala no incluyen corrección por compresión debida a cortes ultrafinos.
Las células de la muestra mostraron una organización macroscópica: las capas corticales se distinguieron claramente por el volumen del soma celular (Fig. 4A). Para encontrar un criterio objetivo de límite de capas, utilizamos el tamaño del soma celular y la densidad de agrupamiento, generando una corteza y sustancia blanca de seis capas (fig. S4; ver materiales y métodos). Las líneas fiduciales en cada panel de la Fig. 4 se basan en estas capas (nombradas en la Fig. 4A). Había menos células con cuerpos celulares grandes en la sustancia blanca y la capa cortical 1 porque estas regiones estaban pobladas principalmente por células gliales con tamaños de cuerpos celulares más pequeños que las neuronas (Fig. 4A, azul). Las células más grandes (Fig. 4A, rojo) se encontraban principalmente en una banda infragranular ancha y profunda correspondiente a la capa 5 y una banda supragranular correspondiente a la capa 3, como era de esperar (37). La forma 3D de las células más sus apariencias de EM permitieron su clasificación en tipos. Los somas celulares más grandes pertenecían a neuronas piramidales espinosas, con variación en el tamaño del soma a lo largo de las capas corticales (Fig. 4C). Las neuronas no piramidales presentaban muchas menos espinas, cuerpos celulares más pequeños y, como grupo, no estaban claramente organizadas en capas (Fig. 4D).
Las células gliales sí mostraron diferencias entre las capas (Fig. 4, E a G). Las arborizaciones compactas y complejas de los astrocitos protoplásmicos se encontraban densamente distribuidas en las capas 2 a 6, como se describió previamente (38-40). Sin embargo, en las partes más superficiales de la capa 1, a menudo estaban más entremezcladas, presentaban una mayor densidad y eran de menor tamaño (Fig. 4E y Fig. S5, A, B y E). Los astrocitos fibrosos en la sustancia blanca eran más alargados que los que ocupaban las capas corticales.
Otros dos tipos de glía, la microglía y las células precursoras de oligodendrocitos (CPO), presentaban una densidad casi uniforme en todas las capas, pero mostraban afinidad por la vasculatura (fig. S5C), a diferencia de los cuerpos celulares de los astrocitos (41). Debido a la similitud morfológica entre las CPO y la microglía, se utilizó un método de aprendizaje automático autosupervisado (SegCLR) para diferenciar estos tipos [véase la sección de materiales y métodos y (42)]. Se predijo que 2517 células eran microglía, 1626 CPO y 2102 no se clasificaron (Fig. 4G y fig. S6).
Otro tipo de glía, los oligodendrocitos (n = 20 139), se distribuían según un gradiente, con la menor densidad en las capas superiores y la mayor en la sustancia blanca, como cabría esperar dado su papel en la formación de mielina (Fig. 4F y fig. S5E).
Al igual que la microglía y las células precursoras de oligodendrocitos (OPC), los oligodendrocitos mostraron afinidad por los vasos sanguíneos (fig. S5C).
Los oligodendrocitos perivasculares formaron líneas a lo largo de los vasos sanguíneos orientados radialmente en la sustancia blanca y, en menor medida, en otras partes del volumen (fig. S5D). La mielina, producto de los oligodendrocitos, siguió el gradiente de densidad de estos, con la mayor densidad en la sustancia blanca y la menor en la capa 2 (fig. 4H y tabla S4). Un número considerable de axones mielinizados discurrían radialmente entre la sustancia blanca y las capas superficiales (fig. 4H, verde) y horizontalmente dentro de las capas en dos ejes ortogonales (fig. 4H, rojo y azul). En la capa 1, un conjunto de axones mielinizados de gran calibre discurrían tangencialmente a través de nuestro corte, paralelos a la piamadre. La mielina en la sustancia blanca discurría principalmente ortogonal al plano de la sección (fig. 4H, azul, y fig. S7). Estas orientaciones de los axones se pueden utilizar para validar las señales de imágenes de tensor de difusión en el cerebro humano in vivo (43, 44).
Los vasos sanguíneos reconstruidos (~230 mm de longitud) no mostraron mucha evidencia de comportamiento específico de capa, pero tenían una densidad menor en las regiones que rodean los vasos grandes y en la sustancia blanca (Fig. 4B), presumiblemente debido a las menores demandas metabólicas de los axones mielinizados de ATP para mantener los gradientes iónicos transmembrana (45). La vasculatura estaba revestida por 4604 células endoteliales (Fig. 4B, verde, ~20/mm de vasculatura) y un grupo más heterogéneo de 3549 pericitos y otros tipos de células perivasculares (Fig. 4B, azul, ~15/mm de vasculatura), también dentro de la membrana basal, pero ligeramente más alejados de la luz (Fig. 4B). Puentes sin sangre (n = 74), compuestos de membrana basal y pericitos, pero sin células endoteliales ni luz (46-48), conectaban diferentes capilares en el conjunto de datos (Fig. 4B, rojo). Desde un punto de vista funcional, un componente crítico del tejido cerebral son sus sinapsis. Mediante un clasificador U-Net, se identificaron ~150 millones de sinapsis y se dividieron en dos categorías: excitatorias e inhibitorias (véase la sección de materiales y métodos). La densidad de las ~111 millones de sinapsis excitatorias fue mayor en las capas 1 y 3 (Fig. 5A), mientras que las ~39 millones de sinapsis inhibitorias alcanzaron su máxima densidad en la capa 1 (Fig. 5B). El porcentaje de sinapsis excitatorias del total [calculado como excitatorias/(excitatorias + inhibitorias)] fue ampliamente similar en todas las capas, siendo ligeramente menor en la capa 1 (Fig. 5C), como se informó previamente (33). La identificación de todas las sinapsis y su asignación a socios pre y postsinápticos específicos permitió la representación de la entrada excitatoria e inhibitoria a cada célula piramidal (Fig. 5D). En la neurona piramidal mostrada en la Fig. 5D, como en otras neuronas excitatorias, las sinapsis en el AIS, el cuerpo celular y las dendritas proximales fueron en su mayoría inhibitorias (azul), mientras que en las regiones dendríticas espinosas, hubo más sinapsis excitatorias (naranja) que inhibitorias. Dicha compartimentalización excitatoria e inhibitoria no fue evidente en las interneuronas (p. ej., véase la Fig. 5E). La comparación de la proporción de entrada excitatoria a inhibitoria en cada capa cortical sobre las neuronas piramidales e interneuronas mostró que el equilibrio excitatorio a inhibitorio variaba ligeramente entre capas, y la mayor proporción de entrada inhibitoria tendía a ocurrir en la capa en la que reside el soma del tipo celular dado (Fig. 5F y tabla S7).
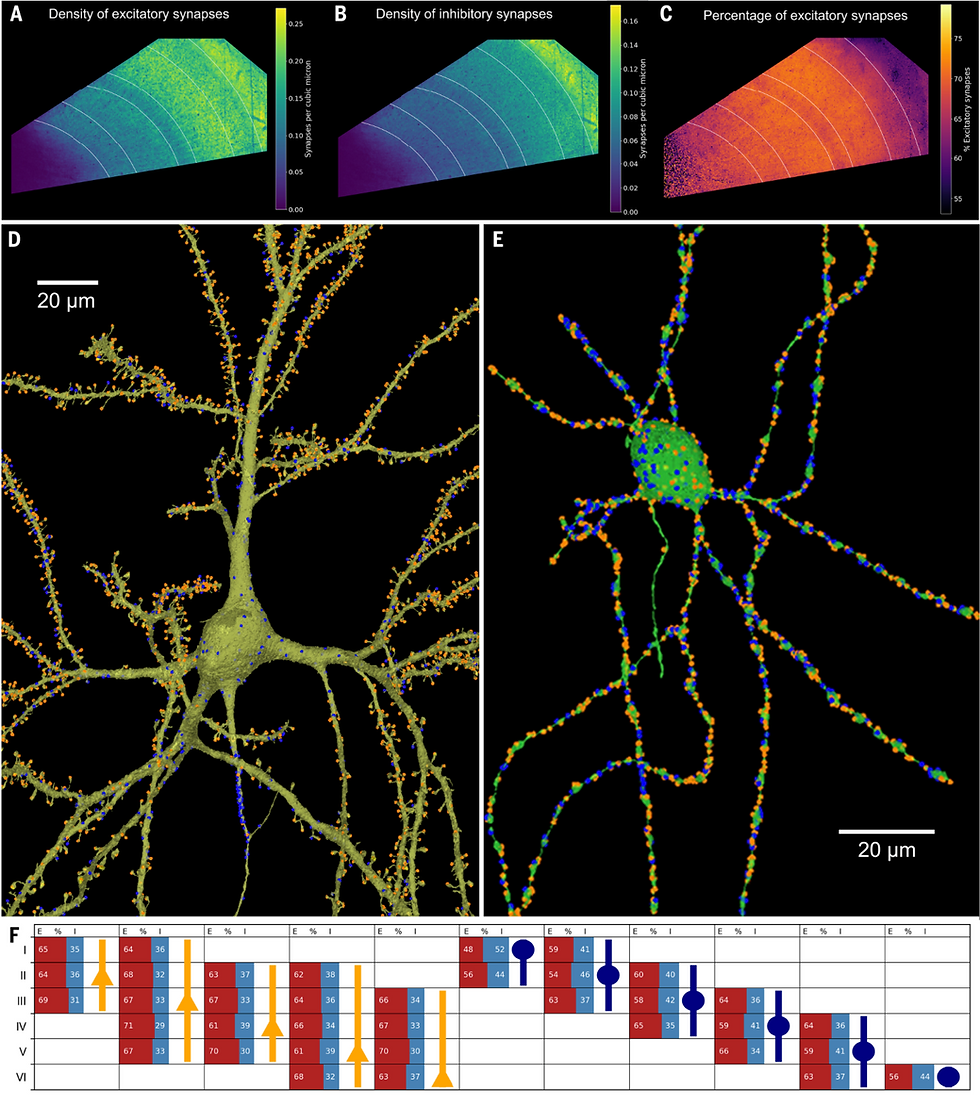
Figura 5. Distribución de sinapsis.
(A) Densidad volumétrica de sinapsis excitatorias (E). (B) Densidad volumétrica de sinapsis inhibitorias (I). (C) Porcentaje de sinapsis excitatorias en diferentes capas (calculado como E/(E + I) * 100%). Los valores más bajos se muestran en morado; los más altos, en amarillo. (D) Neurona piramidal representativa, con sinapsis excitatorias (naranja) e inhibitorias (azul) mostradas. (E) Interneurona representativa. (F) Gráfico de los porcentajes de entradas sinápticas excitatorias (barras rojas) e inhibitorias (barras azules) en diferentes capas corticales (nombres de las filas) para diferentes tipos de neuronas. Los triángulos naranjas representan neuronas piramidales y los círculos azules representan interneuronas; la ubicación de sus filas indica la capa cortical en la que se encuentran sus cuerpos celulares. Se muestran los datos para cada capa cortical en la que al menos
100 células de ese tipo reciben entradas sinápticas.
Para determinar qué tipo de información biológica podría obtenerse del uso de este recurso, examinamos dos fenómenos que encontramos al analizar los datos de imagen.
Subcategorías morfológicas de las neuronas triangulares de la capa 6
La capa más profunda de la corteza cerebral no está tan bien caracterizada como las capas más superficiales (49), en parte porque contiene una mayor diversidad de tipos celulares, especialmente en primates (50). Este recurso proporciona un amplio conjunto de neuronas de la capa profunda y, por lo tanto, puede utilizarse para caracterizar mejor estos tipos celulares. Analizamos las denominadas células "triangulares" o "brújula", que residen en la capa 6 pero que no se comprenden bien (49, 51-53). Estas neuronas espinosas se caracterizan por una dendrita que se dirige hacia el ápice; sin embargo, a diferencia de las neuronas piramidales, cada una tiene una dendrita basal particularmente grande en lugar de una hilera más uniforme de dendritas basales. Identificamos todas las neuronas triangulares en el volumen H01 (Fig. 6A), la mayoría de las cuales se encontraban en las capas 5 y 6 (n = 876), lo que representa aproximadamente un tercio de las neuronas espinosas en estas capas.

Fig. 6. Dos subgrupos simétricos de neuronas triangulares de la capa profunda.
(A) Ubicación de las neuronas con una dendrita apical grande y una dendrita basal grande. El color representa el tamaño del soma celular, como en la Fig. 4A. (B) Distribución de las direcciones de las dendritas basales de las neuronas triangulares, donde la dirección es el ángulo entre la dirección radial y la dirección de la dendrita basal. (C) Vista lateral de las neuronas con dendritas apicales apuntando hacia adelante en la pila z (magenta) o en la dirección inversa (verde claro). (D) Ejemplo de dos neuronas triangulares con dendritas basales apuntando en direcciones opuestas que muestran la simetría especular de estos dos subgrupos. (E) Histograma de los ángulos de las dendritas basales alrededor de la dirección radial. (F) Gráfico polar de los datos en (B) y (E). El verde claro indica las 339 células triangulares con dendritas basales apuntando hacia la sección 0; El magenta indica las 347 células triangulares con dendritas basales apuntando hacia la sección 5292; el gris claro y oscuro indican las 106 y 80 células triangulares, respectivamente, con dendritas basales apuntando lateralmente en el plano de corte. (G) Explicación de la codificación de color direccional en esta figura. (H a J) Agrupación anatómica entre los miembros de los dos subgrupos. (K) Gráfico de barras que compara la dirección de la dendrita basal de cada célula con su vecino más cercano en los datos reales (izquierda) y el control con direcciones de dendritas aleatorizadas (derecha).
Las grandes dendritas basales de las neuronas triangulares emergían de los somas celulares en varios ángulos (de ahí el nombre de "célula brújula"), que iban desde 180° desde la dendrita apical (es decir, hacia la sustancia blanca) hasta ~90° desde la dendrita apical. La orientación media era de ~126° (Fig. 6B). Pudimos agrupar muchas de estas células en dos categorías a lo largo del eje anteroposterior: aquellas en las que la dendrita basal se proyectaba hacia la sección 1 (en la dirección "inversa") y aquellas en las que la dendrita basal se proyectaba en la dirección opuesta ("hacia adelante"), hacia la sección 5292 (células verdes y magenta, respectivamente; Fig. 6, C y D, y vídeo S1). Al tener en cuenta la curvatura de las capas, obtuvimos una dirección promedio de la dendrita apical calculada localmente (es decir, en la "dirección radial" hacia la piamadre; véase la fig. S8). Utilizando estos datos y la orientación de la dendrita basal, observamos que la mayoría (~77,5 %) de las células triangulares se dirigían claramente hacia adelante (n = 347) o hacia atrás (n = 339), formando una distribución bimodal, mientras que el resto presentaba dendritas basales más tangenciales (n = 186; cuatro células eran atípicas con dendritas basales orientadas en dirección radial) (Fig. 6, E a G). El eje formado por estas dendritas basales es el eje principal de los axones mielinizados en la sustancia blanca subyacente, que, según la información disponible, corresponde al eje anteroposterior del lóbulo temporal.
El hecho de que las dendritas basales, en promedio, apuntaran ligeramente hacia la sustancia blanca significaba que los dos conjuntos de dendritas basales no eran paralelos entre sí. En cambio, cada subgrupo presentaba dendritas basales con ángulos simétricos respecto al plano especular (Fig. 6, C y D). Además, encontramos otras características simétricas especulares, como la ausencia relativa de ramificaciones en la parte superior de la dendrita basal y la escasez de ramificaciones dendríticas apicales que apuntan en la misma dirección que la dendrita basal (véase, por ejemplo, la figura 6D).
Al representar los dos subgrupos de neuronas (de proyección anterógrada o retrógrada), observamos que no estaban distribuidos uniformemente. Para evitar sesgos de identificación en el borde de la pila de imágenes, incluimos solo neuronas con cuerpos celulares ubicados en la mitad central del volumen (centrado en las secciones 1323 a 3970; n = 431; Fig. 6, H a J).
A continuación, analizamos la célula triangular vecina más cercana a cada una de estas neuronas y encontramos que su dendrita basal apuntaba en la misma dirección que la dendrita basal de su vecina más cercana con mayor frecuencia de la esperada por azar, lo que muestra una agrupación estadísticamente significativa (Fig. 6K; prueba exacta de Fisher, P = 0,005). Esto indica que estas células se agrupan en cierta medida. Se ha observado una distribución irregular de las proyecciones axonales a la capa 6 en experimentos de marcaje anterógrado en humanos (54). Aún queda por determinar la función de esta distribución bimodal de las direcciones de las dendritas basales de las células triangulares.
Conexiones multisinápticas entre axones y socios postsinápticos específicos
Estudios previos demostraron que los axones en la corteza cerebral de roedores ocasionalmente establecen múltiples sinapsis en la misma célula postsináptica (25, 55). Buscamos determinar si el mismo fenómeno existe en la corteza cerebral humana. Se utilizó CREST para identificar sistemáticamente conexiones fuertes (véase la sección de materiales y métodos para más detalles), donde un solo axón establecía múltiples sinapsis en la misma célula postsináptica. Se encontraron numerosos ejemplos de este fenómeno. Estos incluían axones excitadores e inhibidores que inervaban dendritas postsinápticas excitadoras e inhibidoras en cualquier combinación (Fig. 7, A a D). Estas conexiones fuertes eran poco frecuentes. Para casi todas las células, el histograma del número de sinapsis por entrada axonal mostró una rápida disminución desde la ocurrencia más común, donde un axón establecía una sinapsis con una célula diana (96,49%). Dos contactos sinápticos ocurrieron poco comúnmente (2,99%), se observaron aún menos contactos de tres sinapsis (0,35%), y las conexiones con cuatro o más sinapsis ocurrieron raramente (0,092%; ver tabla S8 para recuentos de entradas a todas las neuronas). Sin embargo, a pesar de la rareza general de conexiones fuertes, encontramos que el 39% de las 2743 neuronas que estaban bien inervadas en el volumen (es decir, que tenían al menos 3000 sinapsis en sus dendritas) tenían al menos una entrada con siete o más sinapsis, lo que plantea la posibilidad de que las entradas axónicas raras y potentes sean una característica general de la inervación neuronal en la corteza cerebral humana. Estos análisis excluyeron los axones de las células candelabro que inervan el AIS, que son bien conocidos por hacer conexiones multisinápticas (56). Cabe señalar también que estos resultados se basan en datos de aglomeración de c3 sin corregir, con muchas divisiones axonales, y por lo tanto, es probable que subestimen la fuerza de las conexiones individuales.

Fig. 7. Conexiones sinápticas inusualmente potentes.
(A) Un axón excitador (verde) forma ocho sinapsis en una dendrita espinosa de una neurona excitadora (púrpura).Una sinapsis es de paso y las demás parecen requerir un crecimiento dirigido del axón para contactar con la mismadendrita. (B) Un axón excitador (azul) forma ocho sinapsis en una dendrita lisa de una neurona inhibidora (verde), de nuevo, con una conexión de paso y las demás aparentemente requiriendo un crecimiento dirigido. (C) Un axón inhibidor (rojo) forma 18 sinapsis en la dendrita apical de una neurona piramidal espinosa excitadora (amarilla azul). (D) Un axón inhibidor (verde) forma nueve sinapsis en la dendrita lisa (amarilla) de otra neurona inhibidora. (E) Un total de 53 conexiones sinápticas desde una neurona piramidal de la capa 3 corregida hacia una
interneurona inhibidora cercana. (F) Gráfico que compara el porcentaje observado (línea roja) y esperado (línea azul) de axones que establecen su conexión más fuerte de entre una y 20 sinapsis con neuronas postsinápticas individuales.
El porcentaje se expresa en escala logarítmica.
Para obtener una descripción más precisa de la frecuencia con la que un axón establece múltiples sinapsis en sus parejas postsinápticas, revisamos el axón y las parejas postsinápticas de una neurona piramidal de la capa 3 que había sido identificada por CREST como capaz de establecer al menos 19 sinapsis en una interneurona cercana. La mayoría de sus parejas postsinápticas (387 de 397; 97,5 %) recibieron uno (72 %), dos (16 %), tres (7 %) o cuatro (2 %) contactos sinápticos de este axón. Estos contactos se formaron generalmente mediante ramificaciones axonales relativamente rectas, aparentemente incidentales a su yuxtaposición con las dendritas que inervaban, lo cual concuerda con la regla de Peters (57). Por el contrario, en ocho puntos donde el axón cruzaba las dendritas de una interneurona inhibidora cercana, estableció un grupo de sinapsis espacialmente restringido en cada punto, dando lugar a un total de 53 sinapsis entre este par de células (Fig. 7E). Este axón excitador también inervaba fuertemente otras cuatro neuronas inhibidoras en su proximidad. Para evaluar si esta neurona piramidal era excepcional, también reconstruimos el axón de una neurona piramidal cercana de la capa 3 y sus 251 parejas postsinápticas. Se encontró que tenía tres conexiones fuertes (más de siete sinapsis), incluyendo 30 sinapsis con una pareja inhibidora y 13 sinapsis con una pareja excitadora (véase la tabla S9 para todos los datos).
Muchas de estas conexiones fuertes compartían una configuración morfológica común. En algunos casos, el axón se cofasciculaba con la dendrita para permanecer en contacto cercano durante decenas de micrómetros, lo que le permitía establecer muchas sinapsis de paso con la misma célula diana (como se muestra en la Fig. 7C). Sin embargo, más comúnmente, el axón no parecía tener una afinidad especial por crecer a lo largo de la dendrita y, en cambio, se acercaba a ella, como era típico de los axones que hacían conexiones de una sola sinapsis, formando una sinapsis en el sitio de intersección sin desviar su trayectoria antes o después de la sinapsis. Además de una sinapsis en el punto de intersección más cercano, estos axones enviaban ramificaciones terminales a la misma célula diana, generalmente a ambos lados de la intersección, lo que sugiere que el axón pudo haber brotado "hacia arriba" para establecer sinapsis en la dendrita y brotado sus ramificaciones terminales "hacia abajo" para establecer sinapsis adicionales con la misma célula diana en el otro lado (Fig. 7, A y B).
Este motivo sugiere un propósito, lo que significa que algunos pares pre- o postsinápticos tenían una razón para estar conectados mucho más fuertemente de lo típico. La posibilidad alternativa es que, dado que miles de entradas axónicas llegan a cada una de las miles de células diana, los resultados atípicos son simplemente parte de la cola larga de una distribución. Por lo tanto, buscamos un modelo nulo conservador para simular el número de axones con conexiones potentes si las conexiones se formaran estocásticamente, basándonos en las trayectorias reales de los axones y las dendritas y las propiedades observadas de las ramificaciones axónicas. El modelo permitió que cada axón simulado formara el mismo número de sinapsis que en los datos reales, pero ahora en cualquiera de las ramificaciones dendríticas que se encontraran en su proximidad para igualar el alcance de los axones reales (véase la sección de materiales y métodos). Nos interesaba ver con qué frecuencia un axón establecería múltiples sinapsis con una sola célula diana. Los resultados indican que este modelo aleatorio de emparejamiento sináptico (Fig. 7F, línea azul) es inconsistente con la incidencia de neuronas fuertemente emparejadas (Fig. 7F, línea roja) que encontramos en H01 (P < 10⁻¹⁰, n = 79.827.631 axones analizados). Esta tendencia de los axones a establecer más sinapsis con ciertas células diana de lo que cabría esperar por azar se mantuvo prácticamente igual al analizar solo axones inhibitorios o solo axones excitatorios (fig. S9).
Por lo tanto, entre un gran número de conexiones incidentales extremadamente débiles, las neuronas de la corteza cerebral humana parecen estar inervadas por un pequeño subconjunto de entradas excitatorias e inhibitorias que establecen conexiones más potentes de forma deliberada.
Discusión. El principio fundamental de la conectómica es capturar tanto la escala macroscópica como la microscópica mediante la reconstrucción de conexiones sinápticas individuales en volúmenes lo suficientemente grandes como para abarcar circuitos neuronales (58). Nuestro objetivo en este trabajo fue crear un recurso que permitiera el estudio de la estructura de la corteza cerebral humana de seis capas con resolución nanométrica dentro de un volumen de aproximadamente un milímetro. Seleccionamos una sección que se extendía desde la capa 1 hasta la sustancia blanca (~3 mm), orientada a lo largo del plano de las dendritas apicales y los axones principales, con la profundidad suficiente (170 µm) para permitir el seguimiento de los axones a través de múltiples capas corticales. La escala nanométrica es necesaria para identificar sinapsis individuales y distinguir entre procesos axónicos y dendríticos densamente empaquetados (59). Adquirimos billones de vóxeles y, por lo tanto, más de un petabyte de datos de imagen digital. Esta cantidad de datos permite visualizar el mismo volumen de tejido cerebral a nivel supracelular, celular y subcelular, así como estudiar las relaciones entre un gran número de neuronas, sinapsis, células gliales y vasos sanguíneos anotados. Quizás lo más importante sea que este recurso ofrece la oportunidad de estudiar las complejas relaciones sinápticas entre numerosas neuronas en una sección de la corteza cerebral de asociación humana.
Para facilitar el estudio, proporcionamos varias herramientas de software. Neuroglancer es una herramienta basada en navegador que permite explorar visualmente el conjunto de datos H01, incluyendo la ultraestructura microscópica, las segmentaciones y las anotaciones de tipos celulares y sinápticos. CREST, una herramienta basada en Neuroglancer, permite explorar las vías sinápticas que convergen o divergen de cualquier neurona en el volumen. CAVE también se basa en Neuroglancer para ofrecer una revisión en línea colaborativa de este conjunto de datos multihaz. Por último, VAST permite a los usuarios exportar, anotar y medir cualquier característica del conjunto de datos mediante esqueletización o pintura de vóxeles.
Utilizando estas herramientas en la muestra H01, descubrimos algunos fenómenos interesantes. Además de varias peculiaridades (fig. S2), encontramos una distinción morfológica entre las células brújula de la capa 6 con dendritas basales orientadas en dos direcciones preferenciales.
También encontramos neuronas que generaban 50 o más sinapsis en parejas postsinápticas individuales. Es posible que se encuentren otras características no descritas previamente tras un análisis más profundo de este conjunto de datos.
El estudio de muestras de cerebro humano presenta desafíos particulares. Si bien el tejido fijado tras un breve período post mortem puede tener la calidad suficiente para permitir la identificación de sinapsis (60), en ocasiones se observan estructuras membranosas sin citoplasma, que no se aprecian en muestras conservadas rápidamente. Afortunadamente, la calidad histológica de la muestra cerebral H01, en cuanto a la visualización de neuronas, glía y sus orgánulos, fue equivalente a la de las muestras cardíacas perfundidas de roedores utilizadas anteriormente (23, 25, 55). Debido a que hubo pocas rupturas de membrana, los datos pudieron reconstruirse tanto manualmente como con aprendizaje automático. Esto sugiere firmemente que la inmersión rápida de tejido fresco en fijador es una alternativa viable a la perfusión y debería ser especialmente útil en estudios de conectómica humana en el futuro (61). Más problemático es que es poco probable que alguna vez se disponga de muestras frescas de individuos sanos a través de esta vía neuroquirúrgica. Aunque el lóbulo temporal de este individuo no mostró cambios patológicos sustanciales por microscopía óptica, como se indica en el informe neuropatológico, es posible que la epilepsia a largo plazo, o su tratamiento con agentes farmacológicos, haya tenido algunos efectos más sutiles en la conectividad o estructura del tejido cortical. Se identificaron algunas rarezas en este tejido, incluyendo varias espinas extremadamente grandes, varicosidades axónicas llenas de material inusual y una pequeña cantidad de axones que formaban espirales extensas (fig. S2). En la actualidad, no podemos determinar si estos resultaron de un proceso patológico o si simplemente son raros. La comparación de muestras obtenidas de individuos con diferentes trastornos subyacentes permitirá comprender mejor los fenómenos observados.
Otro desafío al estudiar el tejido cerebral humano de la corteza de asociación es que sus circuitos probablemente se establecen, al menos en parte, como consecuencia de la experiencia, lo que plantea la cuestión de cuán similar será la corteza de asociación de una persona a la de otra. Si bien existen atlas que describen la variabilidad interindividual de la corteza humana a escalas micro y macroscópicas (62), la falta de conjuntos de datos humanos a escala nanométrica implica que actualmente se desconoce la variabilidad interindividual de los microcircuitos corticales humanos.
Entre nematodos Caenorhabditis elegans individuales con genomas idénticos, aunque la mayoría de las conexiones eran estereotipadas, el 40 % de la conectividad neurona a neurona difería entre individuos (19). Dada la mayor variabilidad en la experiencia, el comportamiento y la genética humanos, y el hecho de que los humanos y otros vertebrados poseen conjuntos de clases de neuronas identificadas (63) en lugar de tipos de neuronas individuales identificados, puede resultar más difícil comparar los circuitos neuronales entre cerebros humanos. Este desafío también presenta una oportunidad para descubrir la instanciación física de la información aprendida. Aunque los circuitos difieran en sus particularidades, es posible encontrar una metalógica de la memoria analizando suficientes datos en el futuro campo de la "engramática" (64, 65).
Sin duda, los enfoques para desentrañar el significado de los datos de conectividad de los circuitos neuronales están en sus inicios, pero este conjunto de datos a escala petaflop representa un buen comienzo.
Resumen de métodos
El tejido resecado del giro temporal medio anterior se sometió a fijación por inmersión rápida y tinción con osmio y otros metales pesados (27). Posteriormente, la muestra se incluyó en resina y se obtuvieron 5019 secciones con un grosor promedio de 33,9 nm mediante un ultramicrótomo automático de cinta (ATUM) (28), lo que resultó en un grosor total de muestra de 0,170 mm. Las secciones se analizaron mediante microscopía electrónica de barrido multihaz con una resolución de 4 × 4 nm (Fig. 1A), obteniéndose un volumen total de imagen de 1,05 mm³ tras corregir una compresión del 28 % en la dirección de corte, y un tamaño de datos brutos de hasta 350 gigabytes por sección, o 1,8 petabytes en total.
De un total de 247 millones de teselas, se unieron 196 millones de teselas de imagen y se alinearon de forma aproximada utilizando las coordenadas de la platina del microscopio y las características de la imagen para relajar una malla triangular elástica de cada tesela y cada sección (Fig. 1B, izquierda). Una alineación de refinamiento a escala fina basada en el flujo óptico entre secciones vecinas eliminó la deriva y la fluctuación restantes del volumen de imagen unificado de aproximadamente 1,4 petabytes (Fig. 1B, centro y derecha).
Se utilizó una red neuronal de filtrado de múltiples resoluciones (FFN) para segmentar los datos de imagen (29), produciendo segmentos base (Fig. 2A) que luego se aglomeraron mediante resegmentación FFN para producir células y procesos reconstruidos más completos (Fig. 2B). Debido a que los errores de aglomeración ocasionales producían fusiones entre objetos cercanos (Fig. 2C, izquierda), esqueletizamos la segmentación y clasificamos los nodos del esqueleto dentro de cada célula como axón, dendrita, astrocito, soma, cilio o AIS (Fig. 2C, centro), lo que permitió realizar un corte automatizado en el sitio de los errores de fusión (Fig. 2C, derecha).
Para identificar sitios sinápticos, entrenamos un clasificador basado en una arquitectura U-Net para etiquetar tres clases: fondo, presináptica y postsináptica (Fig. 2D). Entrenamos un clasificador ResNet-50 de dos clases para clasificar cada sinapsis identificada como excitatoria o inhibitoria según su apariencia en microscopía electrónica, el tipo de estructura postsináptica y el tipo de neurona presináptica, si se conocía.
Agradecimientos
Agradecemos a M. Frosch y S. Huang por su ayuda en la obtención y caracterización de la muestra de tejido cerebral utilizada en este estudio; al equipo multiSEM de Carl Zeiss Microscopy por su ayuda para integrar su dispositivo en nuestro flujo de trabajo; a K. Rockland por su ayuda con la bibliografía pertinente; a J. Choi por su ayuda con la instanciación de CAVE; a los estudiantes A. Judd, E. Pavarino, R. Jiang, R. Han, P. Miao, T. Lu y J. Afeeli por su ayuda con diversos aspectos de este proyecto; y a S. Montgomery por la revisión minuciosa del manuscrito.
Financiación: Este trabajo fue financiado por el Instituto Nacional de Salud Mental de los Institutos Nacionales de Salud (premio del Centro Conte P50 MH094271 a J.W.L.); el Centro Stanley del Instituto Broad (J.W.L.); la Iniciativa BRAIN de los Institutos Nacionales de Salud (subvenciones UG3MH123386, U19 NS104653, U24 NS109102 y UO1 EB026996 a J.W.L.); la Fundación Nacional de Ciencias (subvención NCS-FO-2124179 a H.P. y J.T. y premio NeuroNex 2 2014862 a F.C.); los Institutos Nacionales de Salud (subvención RF1MH125932 a F.C.); y la Actividad de Proyectos de Investigación Avanzada de Inteligencia a través del Departamento del Interior/Centro de Negocios del Interior (contrato D16PC00004 y D16PC0005 a F.C.).
Conflictos de intereses: Los autores declaran no tener conflictos de intereses.
Disponibilidad de datos y materiales: Todos los datos están disponibles en la página web dedicada a este proyecto: http://h01-release.storage.googleapis.com/landing.html, que también incluye enlaces a todo el código utilizado (https://h01-release.storage.googleapis.com/code.html). Todo el código publicado previamente se cita en el texto, incluyendo el de redes de relleno por inundación (29), clasificación de subcompartimentos (66), unión y alineación de imágenes de microscopía electrónica (67) y segmentación volumétrica a partir de datos con anotaciones escasas para la predicción de sinapsis (68). El código no publicado previamente se encuentra archivado en el repositorio Zenodo y se cita en el texto, incluyendo el código MATLAB personalizado utilizado para el análisis (69), el código Python personalizado utilizado para el análisis (70), el código para la verificación automatizada de la calidad de los datos EM (71), el código para el realineamiento a pequeña escala (72) y otros códigos utilizados en este proyecto (73), tal como se cita en la sección de materiales y métodos de los materiales complementarios. El código y las instrucciones para la herramienta CREST están disponibles en línea (74). Los datos de referencia utilizados para entrenar redes neuronales para identificar y clasificar sinapsis están disponibles en Zenodo (75). Los archivos de soporte (en formato zip o original) para cada script se incluyen en el repositorio o, si son extensos, en un repositorio público de Google Cloud Storage, según se indica en el script correspondiente. Varios scripts utilizan bases de datos de Google Cloud BigQuery, que no son de acceso público y requieren un archivo de credenciales para acceder a ellas. Sin embargo, los datos contenidos en estas bases de datos están disponibles para su descarga gratuita en http://h01-release.storage.googleapis.com/data.html. La correspondencia y las solicitudes de materiales deben dirigirse a J.W.L. y V.J.



Comentarios