Fundamentos de Farmacología
- Consejo Mexicano Neurociencias

- 20 ene 2022
- 6 Min. de lectura

La capacidad de un fármaco para producir un efecto en un organismo depende de muchas de sus propiedades, desde su absorción y penetración en los tejidos diana, hasta su estabilidad y su eliminación. Para resumir brevemente estos procesos, el primer factor a tener en cuenta es la vía de administración, que puede determinar la rapidez con la que un fármaco llega a su órgano diana y a qué órganos afecta. La administración oral suele dar lugar a un inicio de acción relativamente lento. La vía parenteral describe todas las demás vías de administración, incluidas la subcutánea (bajo la piel), la intraperitoneal (en la cavidad peritoneal-abdominal), la intravenosa (en el sistema venoso), la intracerebroventricular (en el sistema ventricular cerebral), la intratecal (en el líquido cefalorraquídeo) y la intracerebral (en el parénquima cerebral). La biodisponibilidad de un fármaco se refiere generalmente a la cantidad que entra en la circulación general, lo que a su vez determina la cantidad de fármaco disponible para alcanzar su objetivo. La biodisponibilidad puede verse influida por la absorción del fármaco desde el intestino si se administra por vía oral. También puede verse afectada por la unión del fármaco a las proteínas plasmáticas, lo que hace que el fármaco no esté disponible para unirse a su objetivo. También puede influir la capacidad de un fármaco de penetrar la barrera hematoencefálica si el fármaco actúa en el cerebro (capítulo 2), o su capacidad de permeabilizar las membranas celulares si el fármaco actúa en las proteínas intracelulares. La acción del fármaco también depende de la estabilidad del mismo una vez absorbido, es decir, de la rapidez con la que se metaboliza en congéneres inactivos o se elimina del organismo a través de la orina, la bilis o el aire exhalado.
Algunos fármacos (profármacos) deben convertirse en metabolitos activos antes de poder ejercer sus efectos biológicos. Cada uno de estos factores, que pueden clasificarse como consideraciones farmacocinéticas, es un determinante crítico de la acción de los fármacos e influye tanto en el uso clínico de los mismos como en el proceso de desarrollo de nuevos agentes.
La farmacogenética, que describe la influencia de los genes de un individuo en la determinación de la respuesta a un determinado fármaco, también es fundamental, pero aún se encuentra en las primeras fases de comprensión.
La neurofarmacología está cambiando rápidamente en respuesta a la revolución molecular. En décadas anteriores, la neurofarmacología se centraba en la sinapsis y, más concretamente, en los efectos de los fármacos sobre los neurotransmisores o los receptores de neurotransmisores. La acción de los fármacos sobre las dianas sinápticas sigue siendo un importante campo de investigación. La diana inicial de un fármaco suele determinar las células y los circuitos neuronales concretos sobre los que actúa el fármaco y, al mismo tiempo, la eficacia potencial y los efectos secundarios del agente farmacológico. Sin embargo, la revolución molecular ha dejado claro que la unión inicial de un fármaco a su objetivo -por ejemplo, la unión de un fármaco a un receptor de neurotransmisor- es sólo el comienzo de una cascada de señalización que afecta al comportamiento de las células y, en última instancia, a circuitos complejos.
Cuando un fármaco se une a una proteína, afecta a su funcionamiento. Un fármaco puede unirse a cualquier sitio de una proteína. Un sitio simple puede implicar sólo unos pocos residuos de aminoácidos contiguos en la estructura primaria de una proteína, mientras que un sitio relativamente complejo puede implicar residuos discontinuos de la estructura primaria de la proteína que se acercan entre sí por las estructuras secundarias y terciarias de la proteína. En última instancia, la forma tridimensional, o conformación, de un sitio de unión y las cargas electrostáticas distribuidas por el sitio deben complementar la forma y la carga del fármaco.
La interacción de un fármaco con su sitio de unión puede influir en la actividad intrínseca de la proteína diana, por ejemplo, la actividad catalítica de una enzima o la conductancia de un canal iónico, o puede influir en la capacidad de la proteína para interactuar con alguna otra molécula, como la capacidad de un receptor para unirse a su neurotransmisor. En los estudios clásicos sobre los mecanismos de acción de los fármacos, un mecanismo se define por la capacidad de un fármaco de unirse a un receptor desconocido en homogeneizados de tejido o en secciones de tejido. En estos estudios, el fármaco, denominado ligando, se radiomarca y se incuba con una preparación tisular, que se lava abundantemente para eliminar el fármaco suelto. Hay que añadir un átomo radiactivo al fármaco sin alterar sus propiedades de unión al ligando, un proceso que puede ser excesivamente difícil. La unión del ligando resultante debe ser específica; es decir, el ligando debe unirse a su proteína objetivo específica, que debe distinguirse de la unión a otras proteínas o incluso a la pared de un tubo de ensayo de plástico.
En muchos casos, la unión es estereoselectiva o específica para un solo estereoisómero de un fármaco. La unión también debe ser saturable. Se produce una cantidad limitada de unión del ligando en la preparación porque la cantidad de la diana específica es limitada. (Una preparación tisular contiene una cantidad finita de una proteína receptora individual en comparación con la pared de un tubo de ensayo, que es teóricamente infinita). Además, la unión debe alcanzar un estado estable. El tiempo, la temperatura y otras condiciones de incubación deben permitir que la unión del ligando alcance un estado de equilibrio. El grado de unión de un ligando a una preparación tisular es una función de la concentración del ligando.
La unión total comprende dos componentes (1) la unión específica, que es saturable, y (2) la unión no específica, que no es saturable. En la situación ideal, en la que la unión a un sitio receptor específico es competitiva y totalmente reversible en el estado estacionario, la unión específica puede definirse como la fracción de la unión total que puede desplazarse incubando la mezcla ligando-tejido radiomarcada con un gran exceso de ligando no marcado. Por el contrario, la parte radiactiva no desplazable de la preparación se considera unión inespecífica.

Ensayo de unión del radioligando. En esta representación teórica, la cantidad de radioligando que se une a una preparación tisular (por ejemplo, un homogeneizado, un corte de cerebro) es una función de la concentración del radioligando. La unión total es la cantidad total de unión observada. La unión inespecífica representa la porción no saturable de la unión que presumiblemente no está asociada con el sitio de unión específico investigado; a menudo se calcula como la unión del radioligando que persiste en presencia de un gran exceso de ligando no radiomarcado. La unión específica se calcula como la diferencia entre la unión total y la inespecífica y refleja la cantidad de radioligando unido al sitio de unión específico.
Sin embargo, existen varias discrepancias entre las condiciones ideales y las reales. No todas las uniones a las proteínas diana son realmente reversibles; la afinidad de algunas interacciones ligando-receptor es tan alto que los complejos resultantes no son fácilmente disociables. Además, puede haber sitios artificiales y mostrar una especificidad aparente sorprendente. Mientras que la situación ideal supone que la preparación del tejido contiene sólo una diana específica, en la actualidad muchos fármacos pueden unirse específicamente a muchos subtipos relacionados de una proteína diana; por ejemplo, la serotonina se une a numerosos subtipos de receptores de serotonina. En consecuencia, las curvas de unión resultantes pueden ser bastante complicadas y difíciles de interpretar. La unión específica de un ligando a una preparación tisular se cuantifica según dos propiedades: la afinidad de la unión, que se expresa como una constante de disociación (Kd), y la cantidad total de la unión (Bmax)
Estos términos son análogos a los utilizados en los estudios de cinética enzimática -por ejemplo, la ecuación de Michaelis-Menten- en la que Ka es la constante de activación de una enzima y su cofactor y V",,," es la actividad catalítica máxima de la enzima. La Kd se define como la concentración de ligando a la que se ocupa la mitad de los sitios de unión específicos; los valores de Kd más grandes (por ejemplo, 100 nM frente a 1 nM) reflejan afinidades más bajas del fármaco. Cuando la unión del ligando se representa como una función del logaritmo de la concentración del fármaco, se obtiene una curva sigmoidal.
Los datos de unión del ligando suelen transformarse matemáticamente para obtener un gráfico de Scatchard, en el que la relación entre el ligando unido y el ligando libre se representa como una función del ligando unido (Figura M. Como es difícil medir la cantidad de ligando libre (no unido), el ligando total menos se utiliza el ligando ligado.
La forma de los gráficos de Scatchard proporciona una indicación del número de sitios de unión en una preparación de tejido, así como los valores de Kd y B mar para cada sitio.

Determinación de Kd y B a partir de ensayos de unión de radioligandos. La cantidad de unión específica del radioligando a un sitio específico en una preparación tisular (determinada en 1=11) se traza en función de la concentración del radioligando, utilizando un gráfico normal A o semilogarítmico B. La Kd se calcula como la concentración de radioligando que da lugar al 50% de la unión máxima (Bm). El gráfico semilogarítmico, que ilustra mejor los efectos de las bajas concentraciones de radioligando, sitúa el Kd cerca del centro del gráfico.


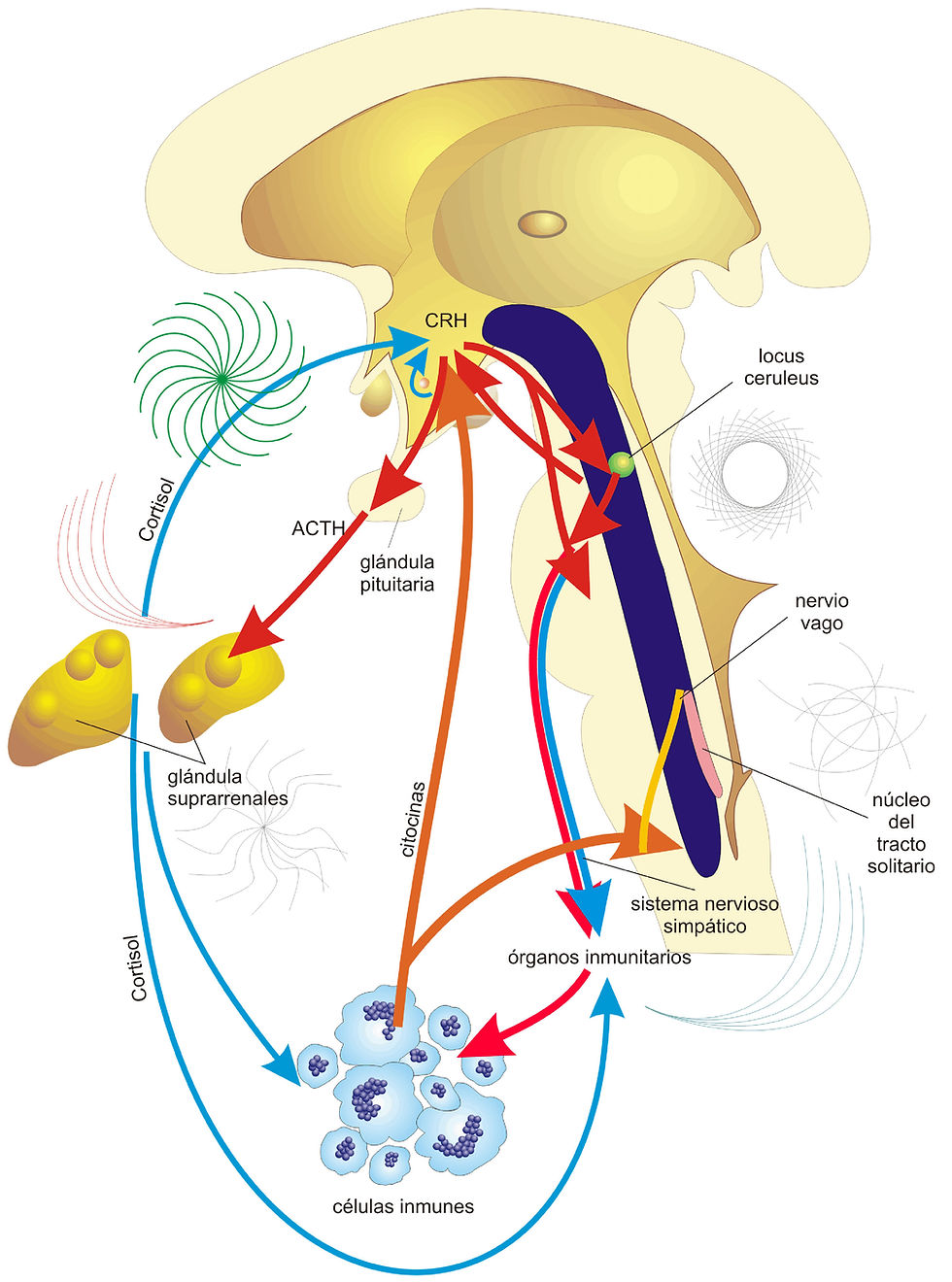

El estudio de la farmacología permite los avnaces sobre que es lo mejor para el bienestar humano, puesto que se fundamenbta que los fármacos cada vez deben ser menos invasivos en cuanto a su absorción y pósiblemas efectos secundarios, a mas de cosnsiderar como actuan nuestro genes frente a los medicamentos, posiblemneste desarrollar dependencia o ressitencia,, Este estudio es de suma importancia para la evolcución en lo referente a tratamientos especificamente por la temática, de enfermedades neurodegenerativas o en el caso de enferdades neuropsiquoiatricas o psicológicas.