DEGENERACIÓN DE LA BARRERA HEMATOENCEFÁLICA IMPLICADA EN LA ENFERMEDAD DE ALZHEIMER
- Consejo Mexicano Neurociencias

- 21 dic 2022
- 13 Min. de lectura

Autores: Jordana Mariane Neyra Chauca, Graciela Gaddy Robles Martínez
RESUMEN
La enfermedad de Alzheimer es una enfermedad neurodegenerativa y por lo tanto esta se produce por una acumulación de placas beta-amiloides por fuera de las células del cerebro y también originada por los ovillos neurofibrilares dentro de las células del cerebro.
Pero al encontrar estos hallazgos en el cerebro y siendo este el órgano más importante del cuerpo humano y susceptible a cualquier cambio, nos preguntamos si existe una estructura que lo proteja y encontramos a una estructura llamada barrera hematoencefálica (BHE), que posee propiedades únicas, estos vasos del SNC en realidad son vasos continuos que no tienen agujeros de permeabilidad, pero también contienen una serie de propiedades adicionales que les permiten regular estrechamente el flujo de moléculas, iones y células entre la sangre y el SNC.
Al conocer su función de la BHE y estudiar su composición histológica, nos damos cuenta que su deterioro tiene una gran implicancia en la aparición y desarrollo de la enfermedad de Alzheimer, pero sobretodo que las posibles causas estudiadas de su deterioro son las mismas que se relacionan con la aparición de la enfermedad de Alzheimer. Sabiendo que la enfermedad de Alzheimer es una enfermedad multifactorial.
Palabras clave: Barrera Hematoencefálica, Alzheimer, Degeneración, Histológico, Microglía, Inflamación, Daño vascular, Estrés oxidativo.
INTRODUCCIÓN
Todos los seres superiores están defendiendo constantemente su integridad biológica frente a una serie de agresiones, esencialmente externas. Así, las células y moléculas del sistema inmunitario llegan a la mayoría de los tejidos a través de la corriente sanguínea, penetrando en los tejidos a través de las paredes de los capilares sanguíneos. Similarmente, el sistema nervioso también penetra en la mayoría de los tejidos, pero ambos sistemas se evitan el uno al otro porque la barrera hematoencefálica impide que los linfocitos (células inmunitarias más conocidas) se pongan en contacto con las neuronas. La razón de ello estriba en que los linfocitos pueden segregar sustancias capaces de destruir las neuronas, con lo que muchos investigadores pensaron en el pasado que el sistema nervioso carecía de protección inmunitaria. Sin embargo, de sobra es conocida la importancia que tiene el sistema nervioso para nuestro correcto funcionamiento. De hecho, es necesario un mecanismo que proteja el sistema que nos da la vida ante infecciones y enfermedades neurodegenerativas, entre ellas el Alzheimer.
Más de 30 millones de personas en el mundo padecen la enfermedad neurodegenerativa de Alzhéimer, según datos de la Organización Mundial de la Salud (OMS) [10].
Un debilitamiento de la BHE que podría permitir una mayor infiltración de beta amiloide en el cerebro, suplementando así la que se produce en el propio cerebro y acelerando el deterioro neuronal, relacionándose así con el inicio del Alzheimer [9].

Datos históricos
Barrera Hematoencefálica
La primera señal de la existencia de la BHE la dio a conocer Paul Ehrlich, en 1885. Ehrlich observó que la inyección de un colorante (por ejemplo, azul de metileno) en la red vascular venosa o en la arterial en el conejo, teñía todos los tejidos del cuerpo del animal, excepto el tejido nervioso. Poco después uno de los colaboradores de Ehrlich, Edwin E. Goldmann, produjo tinción del cerebro, pero no de los tejidos corporales. Ese hallazgo generó estudios para determinar qué factores anatómicos, bioquímicos o fisiológicos intervenían en esa separación entre el tejido cerebral, el líquido cefalorraquídeo y la circulación sanguínea. Fue hasta 1967, gracias a estudios de microscopía electrónica de Karnovsky, Brightman y Reese, que el endotelio capilar del cerebro tenía uniones intercelulares íntimamente unidas y que allí se localizaba la estructura morfológica que conforma la BHE. [3]
Alzheimer
En 1901 fue cuando el psiquiatra alemán Alois Alzheimer identificó el primer caso de lo que se conoce hoy como enfermedad de Alzheimer en una mujer de 51 años de edad. El investigador hizo seguimiento de su paciente hasta su muerte en 1906, y entonces pudo observar el cerebro. Después de este momento pudo reportar públicamente por primera vez el caso. Tras la muerte de la mujer, Alzheimer le examinó el cerebro al microscopio. Anotó las alteraciones de las "neurofibrillas", elementos del citoesqueleto teñidos con una solución de plata [10].
MARCO TEÓRICO
¿Qué es la barrera hematoencefálica?
La barrera hematoencefálica (BHE) es una estructura compleja constituida por células endoteliales de la red capilar del sistema nervioso central (SNC). Además, participan funcionalmente los pericitos, la lámina basal abluminal, los astrocitos perivasculares y la microglía. El endotelio de los capilares cerebrales se caracteriza porque cada borde celular está íntimamente unido a la célula adyacente que hace impermeable a la pared interna del capilar [3].
Composición de la barrera hematoencefálica a nivel histológico
El sellado del endotelio se asocia a tres proteínas: claudina, ocludina y moléculas de adhesión de la unión, y a otras proteínas citoplasmáticas accesorias, tales como ZO1, ZO2, ZO3 y cingulina. La actina también participa. Las claudinas son importantes para la unión estrecha intercelular. Las claudinas – 1 y – 5 con la ocludina forman la BHE. La ocludina es una fosfoproteína. Las moléculas de adhesión de la unión pertenecen a las inmunoglobulinas; aunque hasta ahora no se sabe que papel desempeñan en la BHE [5].

Uniones ocluyentes
Una variedad de juntas especiales, conocidas como uniones ocluyentes o uniones estrechas conectan los espacios entre células endoteliales cerebrales adyacentes. Las uniones ocluyentes están formadas por proteínas que aproximan las membranas celulares. Dentro de las células, estas proteínas se anclan al citoesqueleto (una red de fibras en el interior celular que ayuda a dar y mantener la forma de la célula), mientras tanto, en el exterior celular, ellas interaccionan con otras proteínas de uniones ocluyentes de células vecinas. Como una cinta de doble cara, las uniones ocluyentes unen dos células para evitar el paso de la mayoría de las moléculas y los iones a través del espacio intercelular. [5]
Función de la barrera hematoencefálica
1. Protege al cerebro de los compuestos y las moléculas circulantes en la corriente sanguínea gracias a las bien consolidadas uniones estrechas del endotelio de los capilares cerebrales, lo cual permite que sólo el oxígeno, la glucosa, aminoácidos y otros nutrientes esenciales crucen la BHE.
2. Transporte selectivo desde la red capilar al parénquima cerebral, por medio de transporte facilitado como ocurre con la glucosa, o bien por difusión activa que depende del ATP.
3. La BHE metaboliza o modifica elementos de la sangre hacia el tejido nervioso y viceversa.
En general las sustancias pueden atravesar la BHE por medio de cuatro vías diferentes:
• Penetración por caveolas y transcitosis.
• Difusión transmembranal.
• Mecanismos de acarreo y transportadores.
• Transporte por vía retrógrada de flujo axónico que elude la BHE.
Órganos circunventriculares y BHE
Es necesario mencionar que en el cerebro existen también áreas cuyos capilares tienen endotelio fenestrado, en otras palabras no poseen BHE con el consecuente libre intercambio de moléculas entre la sangre y las neuronas. Esos sitios se localizan principalmente alrededor de las cavidades ventriculares; y por ende son denominados como órganos circunventriculares. En esas estructuras se incluyen el órgano vasculoso de la lámina terminalis (OVLT), el órgano subfornical (OSF), el órgano subcomisural (OSC), la eminencia media, la glándula pineal, la neurohipófisis, y el área postrema (AP). Se debe hacer mención que los plexos coroides han sido excluidos de la lista de órganos circunventriculares aunque no se explica claramente la razón para ello. [10]
Daño de la barrera hematoenecefálica y su implicancia con las enfermedades neurológicas
Varios desórdenes, como infecciones o traumas, pueden causar daño en las uniones ocluyentes y la NVU, destruyendo así la estructura estrechamente tejida de la barrera hematoencefálica. Cuando esto ocurre, el flujo, anteriormente controlado, de moléculas e iones que salían y entraban del cerebro, se vuelve errático [5]. Toxinas, patógenos, o células del sistema inmune pueden entrar en el cerebro, causando inflamación en el CNS. Como respuesta, las células liberan citoquinas (sustancias que son secretadas tras una inflamación o tras la actividad del sistema inmune). Esto altera y degenera las neuronas, lo que conduce al desarrollo de enfermedades neurológicas [6].
Alzheimer
El alzhéimer es una enfermedad neurodegenerativa, esto es, causada por la destrucción de las neuronas cerebrales que se produce por la acumulación en el cerebro de placas de beta-amiloide y proteínas tau, altamente tóxicas para las neuronas [7]. Sin embargo, la razón por la que se inicia esta neurodegeneración no ha sido identificada. Quizás sea, como sugieren algunos estudios, el efecto colateral de la respuesta inmune a una infección cerebral por un virus, una bacteria o un hongo. O podría ser la consecuencia de la apertura de ‘fugas’ en la barrera hematoencefálica [2].
La barrera hematoencefálica y el Alzheimer
La que fuera considerada por mucho tiempo como una enfermedad exclusiva de la tercera edad ha comenzado a detectarse en pacientes muy jóvenes. Se ha comprobado que las adicciones, como el alcoholismo, el tabaquismo y la drogadicción, pueden conllevar su temprana aparición, pues determinadas sustancias se cuelan en el torrente sanguíneo y, debido a su alto nivel tóxico, perturban el comportamiento de la BHE, llegando hasta las neuronas para alterarlas.
Para corroborar todo ello se realizaron resonancias magnéticas cerebrales mejoradas con contraste y las imágenes denotaron que la barrera hematoencefálica que protege el cerebro desarrolla fugas con la edad. Esas fugas comienzan en el hipocampo, un centro importante del aprendizaje y la memoria que está dañado en la enfermedad de Alzheimer. Exámenes post mortem del cerebro de pacientes con enfermedad de Alzheimer también han revelado daños en la barrera hematoencefálica [2]
Comparación entre las causas de la enfermedad de Alzheimer y el deterioro de la barrera hematoencefálica
· Función de la microglía
-Alzheimer
Se caracteriza por provocar demencia y otras alteraciones, pero nuestro objetivo radica en explicar cómo actúa la microglía. Así, una regulación alterada de la microglía podría intervenir también en la enfermedad de Alzheimer. En los cerebros de los enfermos de Alzheimer abundan las placas seniles: regiones anormales en las que depósitos de un fragmento de sustancia amiloide beta (una proteína) se mezclan con la microglía, astrocitos y las terminaciones de neuronas lesionadas. Se supone que estas placas contribuyen a la muerte de las neuronas que subyace en la merma de facultades mentales. Se desconoce de qué modo dañan las células nerviosas. Muchos atribuyen la causa a la sustancia amiloide beta [10].
-Barrera hematoencefálica
Las células de microglía perivascular, diferentes de la microglía de parénquima cerebral se originan en la médula ósea y migran al cerebro. Dado que la microglía es de hecho un macrófago, puede desempeñar funciones importantes en los mecanismos de ruptura de la BHE, en la interfase entre los vasos sanguíneos y el neurópilo, como ocurre en las enfermedades inflamatorias y autoinmunes en los que se incluye la migración transendotelial de monocitos y neutrófilos [5].
Inflamación
-Alzheimer
Varios estudios han demostrado que las personas que toman antiinflamatorios para la artritis tienen menos riesgo de desarrollar el Alzheimer. Las inflamaciones son una reacción del sistema inmune ante las infecciones, las heridas, algunas enfermedades e inclusive la obesidad [4].
La inflamación severa causa fiebre, hinchazón, dolor y enrojecimiento. Sin embargo, la inflamación crónica puede no causar signos externos y este puede ser el caso con el Alzheimer. Se encontró colecciones de células y químicos inflamatorios alrededor de las placas del Alzheimer. Sabemos que una vez que empieza un proceso inflamatorio, los químicos producidos por la inflamación provocan una cascada continua de reacciones. Estos químicos descomponen la membrana celular y esparcen el contenido de la célula, ocasionando su muerte. Este proceso sigue ocasionando la ruptura de más células, lo que resulta en una extensa área de daño [2].
-Barrera hematoencefálica
Desde el punto de vista inmunológico se ha establecido con precisión que la permeabilidad de la BHE aumenta significativamente ante cualquier fenómeno inflamatorio del SNC con la presencia del antígeno correspondiente, lo cual permite la migración al parénquima cerebral de linfocitos T y leucocitos neutrófilos, que caracterizan a la inflamación; los mecanismos moleculares incluyen una serie de factores que conllevan a la ruptura de la BHE en asociación con las células perivasculares, sobre todo, la microglía [5].
· Daño vascular
-Alzheimer
Sorprendentemente, parece haber una relación entre las enfermedades cardiovasculares y el Alzheimer. En 1969, se encontraron niveles elevados de un aminoácido llamado homocisteína en la orina de pacientes con enfermedad cardiovascular. La homocisteína es un residuo normal de la digestión de las proteínas. Si se dan en altas cantidades puede hacer que el colesterol se convierta a su forma “oxidada” y dañe los vasos sanguíneos [2].
-Barrera hematoencefálica
Cualquier evento hipóxico o isquémico va asociado a alteración de las uniones intercelulares y por ende de la BHE, el evento es mediado por citocinas, factor de crecimiento del endotelio vascular (VEGF) y NO. Principalmente aumentan las citocinas inflamatorias, IL-1β y el TNF-α. El aumento de las citocinas y de moléculas de adhesión en las células endoteliales y en los monocitos y neutrófilos conduce a la extravasación de los leucocitos a través del endotelio vascular de la BHE. En otras palabras, la hipoxia/isquemia induce una cascada de eventos, las citocinas, el VEGF, y el NO son los protagonistas, mientras que los astrocitos parecen desempeñar principalmente un papel protector. [6]
· Estrés oxidativo
-Alzheimer
Un estrés suave, experimentado de manera crónica, contribuye a agravar y acelerar los principales rasgos de la enfermedad en las personas, que presentaban una predisposición genética para desarrollar Alzheimer.
Hay muchos estudios que avalan que el estrés produce deterioro cognitivo. Además, los pacientes con depresión tienen episodios de pérdida de memoria y el estrés es uno de los factores que se asocian a la depresión [1].
-Barrera hematoencefálica
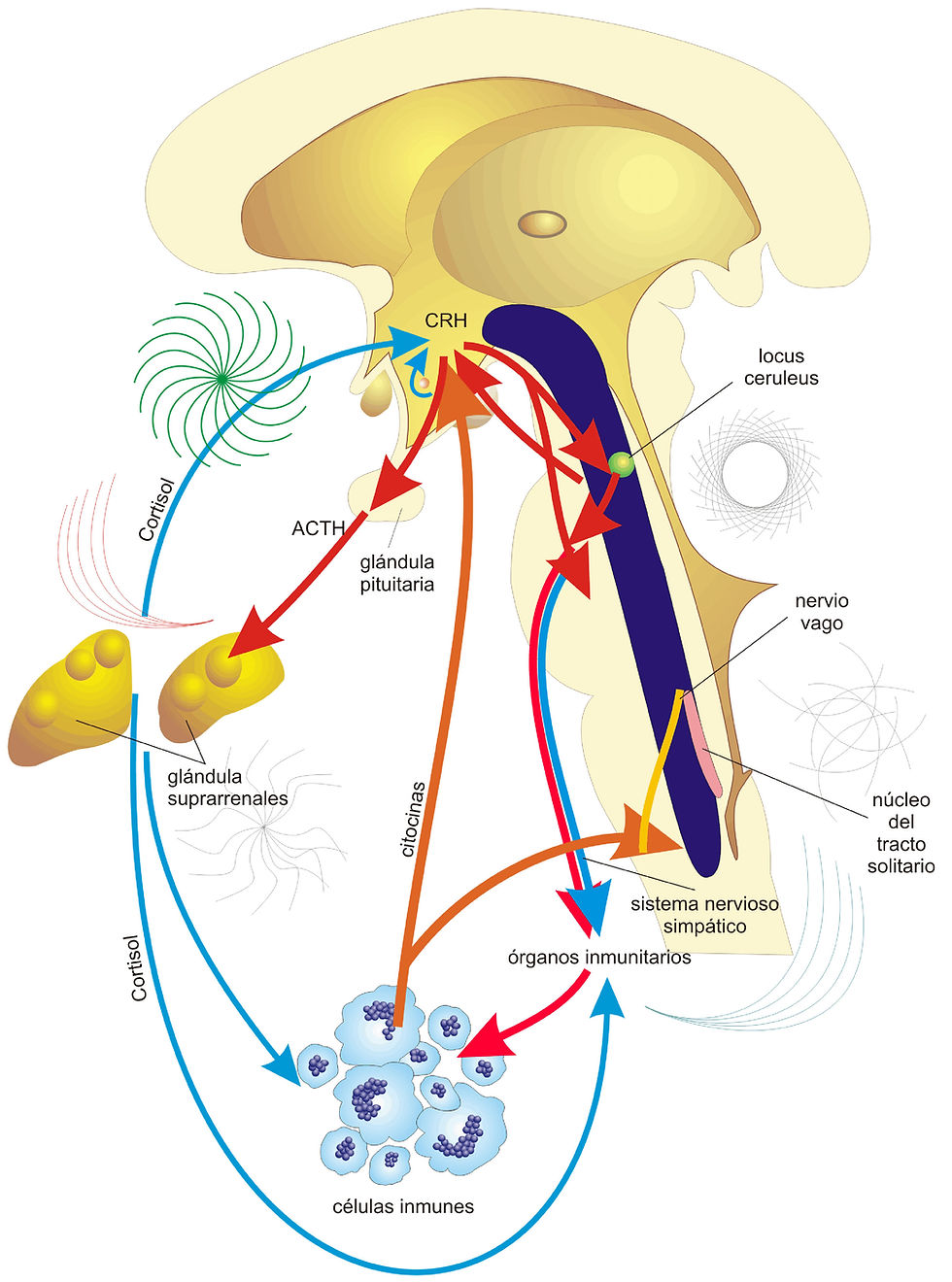
El estrés y las hormonas que se liberan durante la exposición del organismo al mismo, pueden también alterar el funcionamiento normal de la BHE, puesto que la mayoría de las células que participan en la formación de la BHE (células endoteliales, astrocitos, microglía) poseen receptores para glucocorticoides, hormona liberadora de corticotrofina y adrenalina. En el mamífero adulto se sabe que el estrés agudo modifica la permeabilidad de la BHE a moléculas circulantes en la sangre, varios reportes en la literatura describen aumento en la permeabilidad de la BHE después de estrés agudo [5].
Lo que empieza fuera del organismo (parabiosis).
La proteína beta-amiloide cumple numerosas funciones básicas en el organismo. El problema es que cuando adquieren una estructura errónea, estas proteínas se adhieren entre sí formando fibras que, a su vez, se agregarán en oligómeros y placas de beta-amiloide, altamente tóxicas para las neuronas. De hecho, según sugieren numerosos estudios, estas placas son responsables de la muerte de las células cerebrales que desencadenan la enfermedad de Alzheimer. Sin embargo, esta proteína no es exclusiva del cerebro, sino que se produce por todo el cuerpo [4]. Entonces, ¿es posible que la proteína beta-amiloide de origen “extra-cerebral” esté también colaborando en la aparición y progresión del alzhéimer?
Para responder a esta pregunta, los autores recurrieron a una técnica denominada “parabiosis”, en la que dos seres vivos son unidos quirúrgicamente para conformar, cual siameses, un ‘único organismo’ que comparte los sistemas fisiológicos de sus dos predecesores. Y en este caso, utilizaron dos ratones y los ‘cosieron’ para crear un ‘único ratón’ con un sistema circulatorio compartido. El primero de los ratones era totalmente normal y, por tanto, incapaz de desarrollar la enfermedad de Alzheimer. Sin embargo, el segundo ratón había sido genéticamente manipulado para portar una mutación genética responsable de la producción de altos niveles de proteína beta-amiloide. Tal es así que, transcurridos varios meses, presentaba una gran cantidad de placas de beta-amiloide en su cerebro. Y llegado este momento, fue cosido a su homónimo sano durante un año, lo que provocó que los cerebros de ambos animales acabaran compartiendo la enfermedad [9].
DISCUSIÓN
En definitiva, la enfermedad de Alzheimer se origina a partir de la acumulación de proteína beta-amiloide procedente de múltiples partes del organismo, por lo que podría también ser tratada con fármacos que, más allá del cerebro, actúen sobre diferentes órganos. Sería el caso, por ejemplo, de moléculas capaces de unirse a la proteína para que pueda ser eliminada a través del hígado o los riñones.
Nuestros resultados después de haber comprendido y analizado la barrera hematoencefalica desde el punto de vista histológico, sugieren que el incremento de la permeabilidad de esta barrera hematoencefálica podría suponer un mecanismo clave en las fases iniciales de la enfermedad de Alzheimer. No solo por ser una estructura que protege al cerebro, sino por los factores que pueden afectarla y que coinciden con los que afectan al Alzheimer.
Paradójicamente, no ocurre lo mismo con los medicamentos para tratar el alzhéimer: Algunos no son efectivos no por su composición química, sino porque la BHE no permite que atraviesen hacia las células y esto nos produjo una gran inquietud [3], ¿cómo esta estructura puede permitir el paso que agentes extraños o dañinos, pero no el paso de sustancias que actúan como medicamentos para el Alzheimer?, ¿O cuál es la diferencia en la composición de lo que entra al cerebro sin avisar y de lo que pretendemos que entre?, ¿Sera que después de haber sido dañada es capaz de no dejar pasar algunas sustancias y cuál es la razón?, pues son preguntas que aún no podemos resolver ahora, pero seguro que si en un futuro.
Por ejemplo actualmente existen métodos para traspasar la barrera hematoencefalica y actuar directamente en las zonas dañadas que producen el Alzheimer, este método es conocido como las nanopartículas funcionales. [8]
Los científicos creen que para prevenir las demencias, incluyendo la enfermedad de Alzheimer, quizá deban hallarse formas de volver a sellar la barrera hematoencefálica y evitar que el cerebro se vea inundado por las sustancias tóxicas de la sangre [6].
Otra buena noticia según algunos investigadores es que el estrés podría ser un factor de riesgo modificable, tanto a través de programas de reducción y control del estrés percibido, como mediante medicamentos para el control de las hormonas que median en las respuestas al estrés en el organismo: los glucocorticoides. Resulta pertinente señalar que no todos los individuos responden de igual manera ante una situación estresante, y que mientras factores estresantes que aparecen de forma inesperada e impredecible en la vida diaria son tolerados con gran dificultad por muchas personas, otras muestran resiliencia (se adaptan a la situación). Ya hay estudios preclínicos que muestran que estos individuos resistentes al estrés podrían ser resistentes al desarrollo de la enfermedad de Alzheimer. [1]
CONCLUSIÓN
Conocer la relación de una manera tan profunda entre estructuras del cuerpo humano incluso microscópicas, estudiarlas a nivel histológico como es el caso de la barrera hematoencefalica y relacionarlas con patologías actuales, de gran impacto mundial como el Alzheimer es muy enriquecedor para nosotros como estudiantes de medicina. Sobre todo para aquellos que nos gusta la investigación y tomando una enfermedad como el Alzheimer que es considerada una enfermedad multifactorial y que aun los científicos continúan la ardua tarea de buscar las causas exactas de su origen, nos llena de satisfacción acercarnos un poco más a la comprensión de esta patología. Por eso estudiando e identificando la anatomía como primer paso ubicamos las lesiones que produce esta enfermedad que sería en el cerebro específicamente.
Luego estudiamos las estructuras implicadas en la protección del mismo, reconocemos sus funciones, su composición y cuáles son los factores que están implicados en su deterioro hablando, nos referimos la barrera hematoencefalica y relacionarlos con las enfermedades neurodegenerativas en general, pero avocándonos al Alzheimer por los estudios ya realizados anteriormente por expertos y por medio nuestro análisis identificando, comparando, profundizando sobre aspectos que comparten estos conceptos médicos relevantes.
REFERENCIAS BIBLIOGRÁFICAS
1. Navarra U, Nutrición F, opinión A. Estrés crónico y Alzheimer, una relación dañina [Internet]. Unav.edu. 2016 [cited 3 May 2019]. Available from: https://www.unav.edu/web/facultad-de-farmacia/detalle-opinion/2016/09/21/estres-cronico-y-alzheimer-una-relacion-da%C3%B1ina/-/asset_publisher/NuB2/content/2016_09_21_opinion_far_alzheimer/10174
2. Dean C. El Gran Libro de la Enfermedad de Alzheimer. 1st ed. Bogota, Colombia: Panamericana Editorial Ltda; 2011.
3. Sossa B. D, Bazyar S. Permeabilidad de la barrera hematoencefálica en tumores endocraneanos evaluada con técnica de realce dinámico con contraste - T1W IRM. Serie de casos [Internet]. studylib.es. 2014 [cited 3 May 2019]. Available from: https://studylib.es/doc/4863307/permeabilidad-de-la-barrera-hematoencef%C3%A1lica-en-tumores
4. Gutierrez Robledo L, Rojas Mayorquin A, Gutierrez Avila J, Ortuño Sahagun D. Tópicos de actualización en neurobiología: Envejecimiento y Neurodegeneración. 1st ed. Guadalajara, Jalisco, Ciudad de México; 2011.
5. Pascual-Garvi J, Gonzalez-LLanos E, Prieto-Arribas R. La barrera hematoencefálica: desarrollo de una estructura que permite la heterogeneidad funcional del sistema nervioso central [Internet]. studylib.es. 2004 [cited 3 May 2019]. Available from: https://studylib.es/doc/5351048/la-barrera-hematoencef%C3%A1lica--desarrollo-de-una-estructura...
6. Dominguez Ortega F, González Azpeitia G, Cidrás Pidre M, Calvo Rosales J. Apertura reversible de la barrera hematoencefálica inducida por hipercapnia en hiperbilirrubinemia experimental [Internet]. Aeped.es. 1997 [cited 3 May 2019]. Available from: https://www.aeped.es/sites/default/files/anales/46-4-13.pdf
7. Gra Menendez S, Padrón Perez N, Llibre Rodriguez J. PÉPTIDO BETA AMILOIDE, PROTEÍNA TAU Y ENFERMEDAD DE ALZHEIMER [Internet]. Docplayer.es. 2002 [cited 3 May 2019]. Available from: https://docplayer.es/7049230-Peptido-beta-amiloide-proteina-tau-y-enfermedad-de-alzheimer.html
8. Rodriguez Torrado M, Fernández Carballido A. Nanopartículas funcionalizadas para favorecer su paso por la BHE [Internet]. 147.96.70.122. 2016 [cited 3 May 2019].Available from: http://147.96.70.122/Web/TFG/TFG/Memoria/MARTA%20RODRIGUEZ%20TORRADO.pdf
9. Ruíz Sandoval J, Otero Siliceo E. Aspectos bioquímicos en la enfermedad de Alzheimer [Internet].Imbiomed.com.mx. 1997 [cited 3 May 2019]. Available from: http://www.imbiomed.com.mx/1/1/articulos.php?method=showDetail&id_articulo=4900&id_seccion=21&id_ejemplar=539&id_revista=5
10.Peña-Casanova J. Enfermedad de Alzheimer del diagnóstico a la terapia: conceptos y hechos. 1st ed. Barcelona: Fundación La Caixa; 1999.



😍Gracias por tan valiosa informacion